الکل
الکل
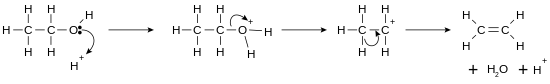
در شیمی به هر ترکیب شیمیایی که یک گروهِ هیدرکسیل (-OH) متصل به کربن یک آلکیل داشتهباشد، الکل گویند. فرمول کلی یک الکل سادهٔ غیر حلقهای CnH2n+1OH است. در شیمی الکلها در شمار گروه مهمی از ترکیبهای شیمیایی هستند و در واکنشهای گستردهای شرکت میکنند و بسیاری از ترکیبهای شیمیایی از آنها به دست میآیند، به طوری در کتاب شیمی آلی موریسن و بوید آمدهاست که اگر به شیمیدانی بگویند او را با ده ترکیب شیمیایی دریک جزیره تنها خواهند گذاشت الکل یکی از آنها خواهدبود.
به طور کلی، زمانی که نام الکل به تنهایی به کار میرود، معمولاً منظور اتانول است که همان الکل گرفتهشده از جو یا عرق یا همان مشروبات الکلی میباشد. اتانول مایعی بیرنگ و فرار وبا بویی بسیار تند است که از تخمیر شکرها به دست میآید. همچنین گاه به هر گونه نوشیدنی که الکل داشتهباشد، الکل میگویند. هزاران سال است که معمولاً الکل به عنوان یکی از عاملهای اعتیادآور به شمار میآید.
الکلهای دیگر بیشتر با صفتهای مشخصکنندهٔ ویژهٔ خود میآیند مانند الکل چوب (که همان متانول است) یا ایزوپروپیل الکل. پسوند «ول» نیز در پایان نام شیمیایی همهٔ الکلها میآید.
تاریخچه[ویرایش]
الکل را زکریای رازی پزشک ایرانی کشف کرد[نیازمند منبع]
ساختار و دستهبندی[ویرایش]
الکلها بسته به نوع کربن[۱] که به گروه OH- پیوند دارد، به سه دسته نوع اول، نوع دوم یا نوع سوم طبقهبندی میشوند: 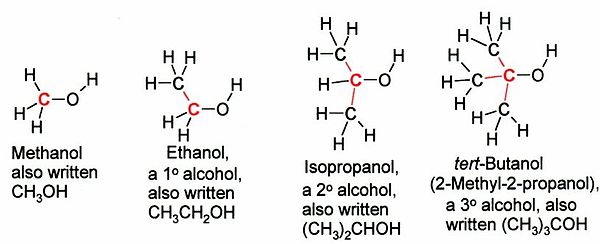
نمایش کلی انواع الکل[ویرایش]
- الکل نوع اول CR(H)۲-OH.
- الکل نوع دوم C(R)۲H-OH.
- الکل نوع سومC(R)۳-OH.
خواص فیزیکی الکلها[ویرایش]
دمای جوش[ویرایش]
الکلها در میان هیدروکربنهای هم وزن خود دمای جوش بالاتری دارند که آن را میتوان به پیوند هیدروژنی الکلها دانست
حلالیت[ویرایش]
با توجه به این که پیوند بین الکلها مانند آب، پیوند هیدروژنی است به هر اندازهای در آب حل میشود. همچنین با توجه به این که الکلها از یک سو بخشی آلی داشته و از سوی دیگر گروه هیدروکسید دارند بسیاری از مواد آلی را نیز حل میکنند.
محلول ید در محلول آب و الکل را تنتورید میگویند و برای گندزدایی به کار میروند.
سمشناسی[ویرایش]
الکلها بیشتر بویی تند و زننده دارند و اتانول از دوران پیش از تاریخ به دلیلهای گوناگون بهداشتی، رژیمی، مذهبی و تفریحی به عنوان نوشیدنی الکلی به کار میرفتهاست. هرچند استفادهٔ کم و گهگاه الکل میتواند بیزیان باشد، اندازههای بیشتر آن سبب مستی شده و در مقدارهای بیشتر میتواند به اختلالات تنفسی و حتی مرگ نیز بینجامد.[۱]
الکلهای دیگر سمیتر از اتانول هستند، که این نیز بیشتر به دلیل نیاز به زمان بیشتر برای تغییر در فرایند سوخت و ساز است و حتی گاه در فرایندهای دگرگشت (متابولیسم) مادههایی سمی میسازند. برای نمونه متانول، که همان الکل چوب است، به وسیلهٔ آنزیمها در جگر اکسایش مییابد و مادهٔ سمی فرمالدهید تولید میکند که میتواند سبب کوری یا مرگ شود.
یکی از راههای کارا در پیشگیری از سمیت فرمالدهید، فراهم آوردن اتانول در کنار آن است چون آنزیمهای هیدروژنزدایی که از متانول فرمالدهید میدهند بر اتانول اثر بیشتری دارند، بدین گونه از پیوند و عمل بر روی متانول پیشگیری میکند. در این زمان متانول باقیمانده وقت دفع از راه کلیهها را پیدا کرده و فرمالدهید باقیمانده نیز به فرمیک اسید تبدیل میشود.
نامگذاری[ویرایش]
|
سدیم لورت سولفات
| سدیم لورت سولفات | |
|---|---|
| شناساگرها | |
| کوتهنوشتها | SLES |
| شماره ثبت سیایاس | ۹۰۰۴-۸۲-۴ |
| خصوصیات | |
| فرمول مولکولی | CH3(CH2)11(OCH2CH2)nOSO3Na |
| جرم مولی | حدود 420 g/mol (288.38 + 44.05n) g mol−1 |
| خطرات | |
| لوزی آتش |  |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| | |
| Infobox references | |
سدیم لورت سولفات (به انگلیسی: Sodium laureth sulfate) با نام اختصاری SLES[۱] و با فرمول شیمیایی CH۳(CH۲)۱۰CH۲(OCH۲CH۲)nOSO۳NaC12+2nH25+4nNaO4+nS یک ترکیب شیمیایی است؛ که جرم مولی آن ۴۲۰ g/mol میباشد.این ماده یک ماده فعال سطحی است که در بسیاری از شویندههای مصنوعی از جمله صابون، شامپو و خمیردندان مشاهده میشود.
آهک
آهک یک نوع هیدرات کلسیم است. که در واقع یک جسم سفید رنگ و جاذب رطوبت می باشد که از پخت سنگ آهک به دست می آید .
استن
استن یک ماده شیمیایی و لکه بر است . این ماده فرار و به شدت آتش گیر است . و مصرف زیادی در صنعت به عنوان حلال دارد .یکی از روش های ساده برای ساخت استن تقطیر استات کلسیم می باشد .
کاغذ تورنسل یا کاغذ لیتموس
کاغذ تورنسل یا کاغذ لیتموس (به انگلیسی: Litmus) یکی از شناساگرهای محیط میباشد و برای شناسایی اسیدها و بازها استفاده می شود. کاغذ لیتموس به دو رنگ موجود است لیتموس آبی و لیتموس قرمز، از لیتموس آبی برای محیط اسیدی و از لیتموس قرمز برای محیط بازی استفاده می کنند. کاغذ آبی تورنسل در محیط اسیدی قرمز می شود و کاغذ قرمز تورنسل در محیط بازی آبی می شود . محلول تورنسل نیز در pH کمتر از 4.5 قرمز و در pH بالای 8.3 آبی و در محدوده دو pH که محدوده خنثی برای این شناساگر است بنفش می باشد .